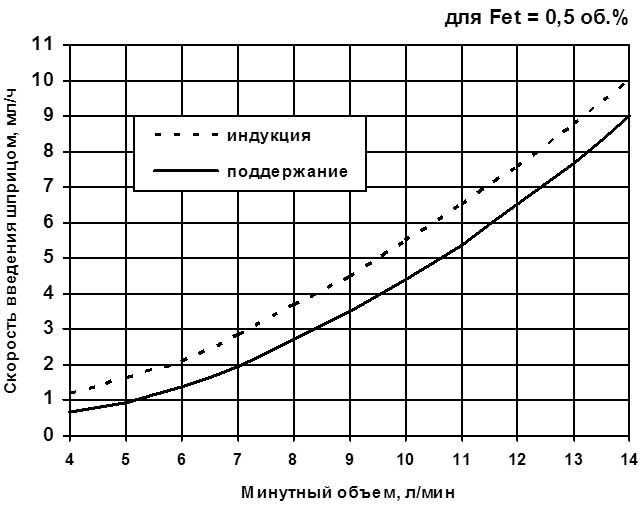
Фармакологические свойства севофлурана и изофлурана
Фармакодинамика
Вводная анестезия севофлураном характеризуется отсутствием раздражения верхних дыхательных путей, не вызывает избыточную секрецию в трахеобронхиальном дереве и стимуляцию центральной нервной системы. В отличие от севофлурана, изофлуран не рекомендуется для вводной анестезии через маску наркозно-дыхательного аппарата из-за раздражающего действия на дыхательные пути, тем не менее, препарат не вызывает усиление слюноотделения или трахеобронхиальной секреции. При этом фарингеальные и ларингеальные рефлексы быстро подавляются.
Ингаляционные анестетики вызывают дозозависимую респираторную депрессию: снижение дыхательного объема, чувствительности к углекислому газу и гипоксии, увеличение частоты дыхания. Данные препараты способны уменьшать бронхоспазм, вызванный действием ацетилхолина и гистамина. Бронходилатирующий эффект обусловлен воздействием на трансмембранный транспорт кальция и вегетативную иннервацию, в том числе на секрецию ацетилхолина. Бронходилатирующий эффект у изофлурана выражен больше, чем у севофлурана.
Основное и целевое действие изфофлурана и севофлурана на центральную нервную систему, позволяющее применять их для седации — это сочетание гипнотического и иммобилизирующего эффектов. Севофлуран оказывает минимальное действие на внутричерепное давление и не снижает реакцию на углекислый газ. Для пациентов с массивными внутричерепными повреждениями существует риск ишемии или вклинения головного мозга при повышении внутричерепного давления, а для пациентов с цереброваскулярной недостаточностью актуальна проблема поддержания достаточного мозгового кровотока.
Севофлуран и изофлуран, как и другие ингаляционные анестетики, оказывают двойное действие на церебральные сосуды: при низкой концентрации (супрессия метаболизма) возникает вазоконстрикция, при высокой — вазодилатация. Севофлуран дозозависимо повышает общий мозговой кровоток и снижает мозговое сосудистое сопротивление. Изофлуран обладает большей способностью поддерживать общий мозговой кровоток в соответствии с метаболической потребностью в кислороде, чем севофлуран.
Ингаляционные анестетики, вызывая прямой вазодилятационный эффект в головном мозге, могут также изменять ауторегуляцию кровотока в ответ на метаболические потребности, то есть нарушать соотношение «кровоток–метаболизм» в пользу кровотока. Кроме того, на ауторегуляцию церебрального кровотока может влиять снижение системного артериального давления, вызванное вазодилатацией. У людей севофлуран и изофлуран уменьшают потребление кислорода мозгом.
Все галогенсодержащие анестетики вызывают дозозависимое снижение среднего артериального давления, обусловленное уменьшением общего периферического сосудистого сопротивления за счет воздействия на симпатическую систему, но без заметного влияния на сердечный выброс.
Итак, севофлуран и изофлуран в клинически используемых концентрациях не вызывают снижения сердечного выброса. Однако, как и все парообразующие анестетики, они обладают отрицательным инотропным эффектом. Способность севофлурана и изофлурана уменьшать общее периферическое сосудистое сопротивление при сохраненном сердечном выбросе может объяснить поддержание хорошего регионарного кровотока в важнейших органах. Эти препараты не вызывают повышения чувствительности миокарда к адреналину и предрасположенности к вентрикулярным нарушениям ритма и, кроме того, могут предупреждать аритмогенные последствия ишемии миокарда. Тем не менее, следует контролировать дозу и скорость введения адреналина и содержащих его анестетиков во время ингаляционной анестезии или седации.
Фармакокинетика
Как известно, анестетическая сила севофлурана наполовину меньше, чем у изофлурана. Равновесное состояние в течение 30 мин в альвеолах достигается быстро: севофлурана на 85%, изофлурана — на 73%. Выведение ингаляционных анестетиков определяется их растворимостью в крови, при этом соединения с более низкой растворимостью, выводятся из тканей быстрее. В течение первых двух часов после прекращения общей анестезии выведение севофлурана происходит приблизительно в 1,6 раз быстрее, чем изофлурана.
Изофлуран подвергается относительно небольшому метаболизму в организме человека. После завершения седации или анестезии, в виде метаболитов в моче обнаруживают только 0,17% изофлурана. Пиковая сывороточная концентрация неорганического фтора обычно составляет менее 5 мкмоль/л и наблюдается через 4 часа после анестезии. Уровень фтора возвращается к норме в течение 24 часов. Признаков повреждения почек после применения изофлурана зарегистрировано не было. Известные метаболиты изофлурана не обладают токсичностью или определяются в слишком низких концентрациях.
При распаде севофлурана образуются полифторированые галоалкены, в основном, пентафторизопропенилфтор-метиловый эфир, известный так же, как «Соединение А». Быстрое выведение севофлурана из легких сводит к минимуму метаболизм препарата.
У человека менее 5% севофлурана метаболизируется под действием цитохрома Р450 (CYP 2E1) в гексафторизопропанол с высвобождением неорганического фтора и диоксида углерода. Образующийся гексафторизопропанол быстро конъюгируется с глюкуроновой кислотой и выводится с мочой. Другие пути метаболизма севофлурана не установлены. Этот препарат является единственным фторированным летучим средством для наркоза, не метаболизирующимся до трифторуксусной кислоты. По этой причине севофлурану не свойственна гепатотоксичность.
Изофлуран образует трифторацетат в процессе биодеградации, однако в силу значительно меньшей биотрансформации существенно реже вызывают острый некроз печени. Описаны лишь несколько случаев возникновения острого некроза печени после анестезии изофлураном.

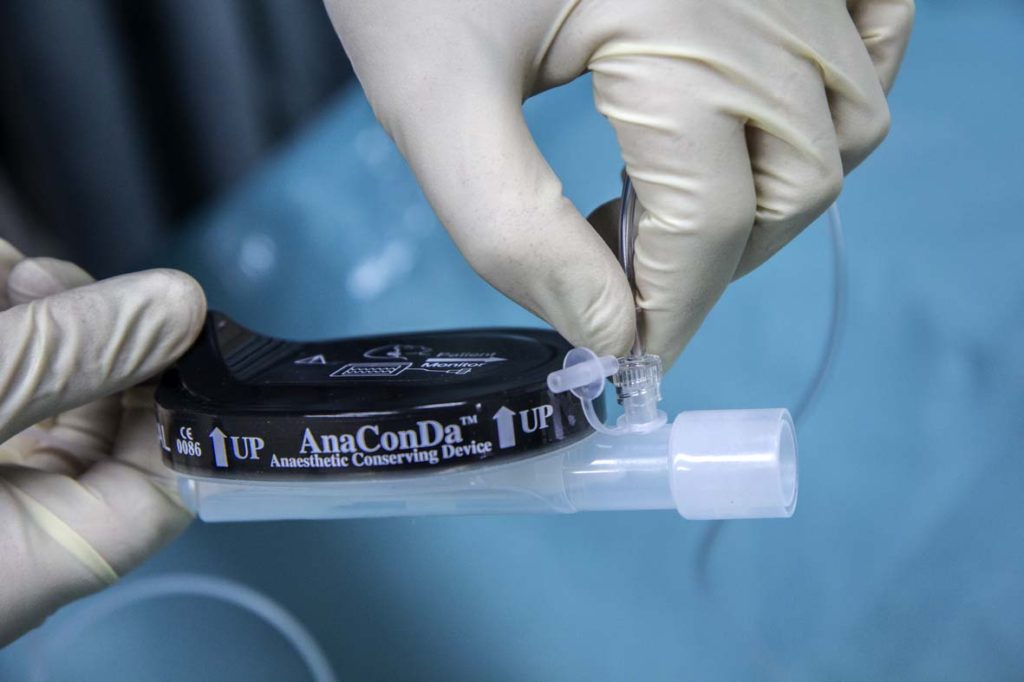
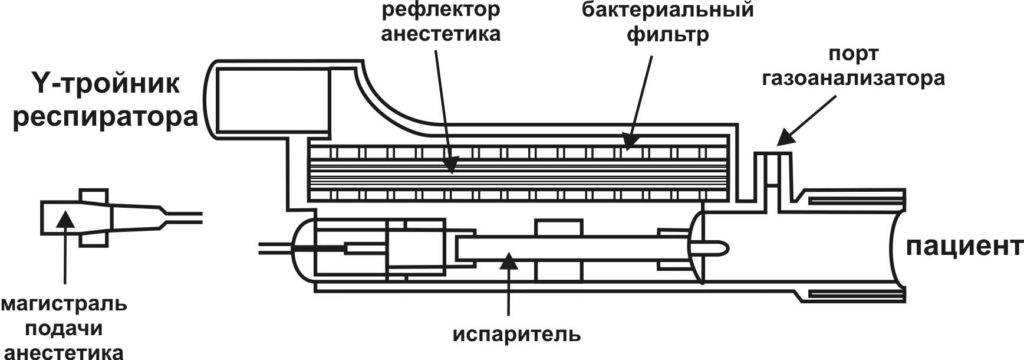


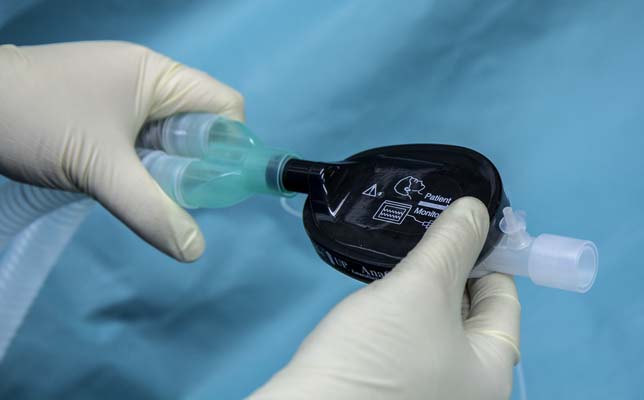
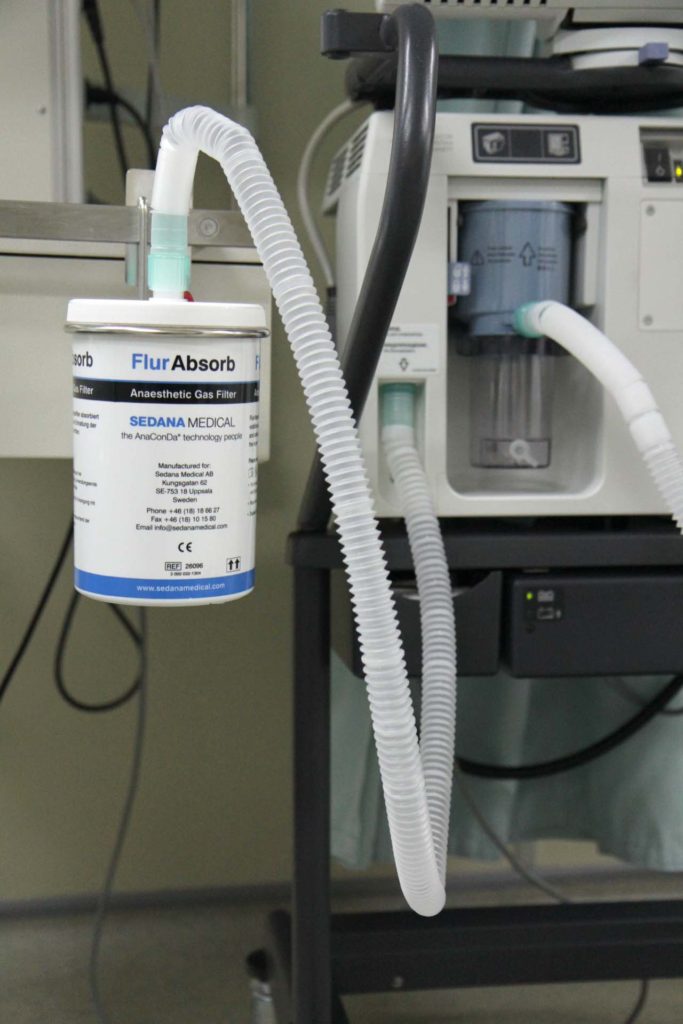 Рисунок 4. Установка фильтра остаточного газа на аппарат ИВЛ
Рисунок 4. Установка фильтра остаточного газа на аппарат ИВЛ